VALIDAR LA CALIDAD ANALITICA
|
|
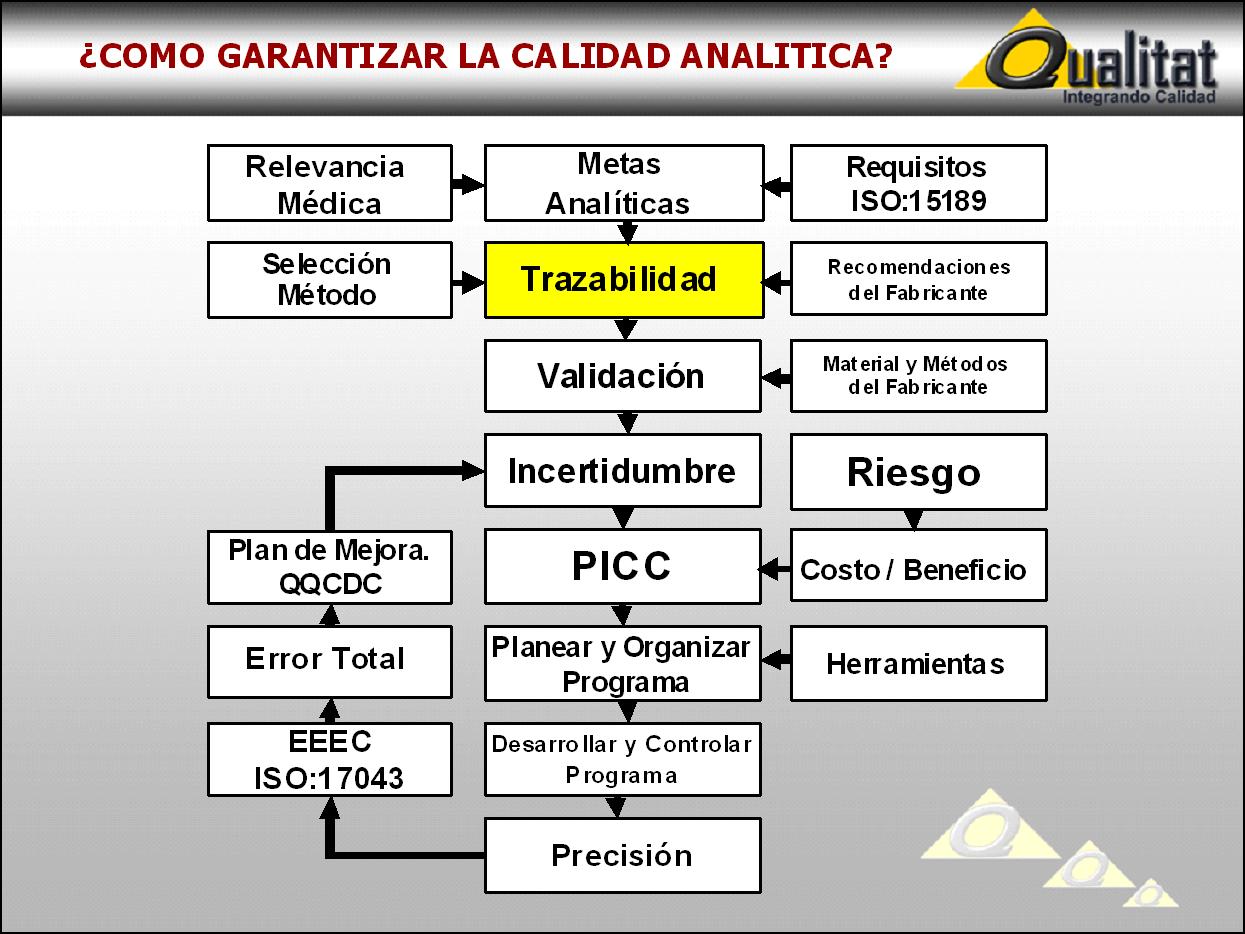
TRAZABILIDAD METROLOGICA Y VALIDACION ANALITICA
LA RELEVANCIA MEDICA ES LA PREMISA FUNDAMENTAL 1. La validación debe considerar los aspectos de confiabilidad y de aplicabilidad que pueden comprometer la calidad de las mediciones. a) La confiabilidad es inversamente proporcional a la incertidumbre. b) La aplicabilidad es inversamente proporcional al costo / beneficio, en función de tiempo, dinero y esfuerzo. 2. Las características del confiabilidad analítico a considerar son: a. Precisión b. Exactitud c. Linealidad d. Limite de detección e. Rango analítico f. Interferencias analíticas g. Acarreo h. Sensibilidad analítica i. Especificidad analítica j. Error analítico total 3. Las características de aplicabilidad que conviene considerar son: a. Costo por prueba incluyendo costos directos e indirectos, aparentes y ocultos. b. Versatilidad del instrumento c. Volumen de la muestra d. Tiempo de respuesta urgencias y rutina. Disponibilidad las 24 hrs del dia. d. Destreza requerida por parte del operador. Capacitación. e. Procedimientos de mantenimiento y limpieza g. Flexibilidad (amigable) h. Respuesta de servicio del proveedor incluyendo disponibilidad de insumos y de mantenimiento. 4. Existen protocolos de validación publicados por CLSI: Clinical and Laboratory Standards Institute (Antes NCCLS) a. EP05-A2: Evaluation of Precision Performance of Quantitative Measurement Methods; Approved-Second Edition. (2004) b. EP06-A : Evaluation of the Linearity of Quantitative Measurement Procedures: A Statistical Approach; Approved Guideline. (2003) c. EP07-A: Interference Testing in Clinical Chemistry; Approved Guideline (2002) d. EP09-A2 : Method Comparision and Bias Estimation Using Patient Samples;Approved Guideline - Second Edition (2002) e. EP10-A2: Preliminary Evaluation of Quantitative Clinical Laboratory Methods; Approved Guideline - Second Edition (2002) f. EP12-A: User Protocol for Evaluation of Qualitative Test Performance; Approved Guideline (2002) g. EP14-A : Evaluation of Matrix Effects; Approved Guideline (2001) h. EP15-A : User Demonstration of Performance for Precision and Accuracy;Approved Guideline (2001) i. EP17-A : Protocols for Determination of Limits of Detection and Limits of Quantitation; Approved Guideline j. EP21-A : Estimation of Total Analytical Error for Clinical Laboratory Methods; Approved Guideline (2003) LA MISION DE QUALITAT ES LA DE COLABORAR CON LOS PROFESIONALES DEL LABORATORIO CLINICO EN LA DETECCION CONFIABLE DE LAS OPORTUNIDADES DE MEJORA PROPORCIONANDO ASESORIA, ASISTENCIA TECNICA Y CAPACITACION VALIDACIÓN Diccionario de la lengua española
© 2005 Espasa-Calpe: Hacer válido, dar fuerza o firmeza
DESCARGAR FORMATO PARAMETRIZACION < >
TRAZABILIDAD,VERIFICACION Y VALIDACION: ACCESAR TUTORIAL < > ACCESAR SW PARA LA VALIDACION ANALITICA QC PROCESS < > ACCESAR FORMATO QC PROCESS < >
< > ISO17043. CRITERIOS DE APLICACION. ema.ac. < > POLITICA ema.ac.INCERTIDUMBRE DE LAS MEDICIONES < > CENAM, ema.ac. GUIA PARA LA VALIDACION Y VERIFICACION DE PROCEDIMIENTOS
EN EL SIGUIENTE CUADRO SE PUEDE OBSERVAR QUE SOLO EXISTE CONTROL TOTAL R = 1.0 A LO LARGO DEL RANGO ANALITICO EN UNA DE LAS DOCE GRÁFICAS DONDE Y = mX + b m= pendiente b = ordenada origen
VALIDE SUS RESULTADOS DEL EEEC UTILIZANDO LA HERRAMIENTA PARA CONTROL DE EXACTITUD |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||